10秒サマリー
- Stanford A型:上行大動脈に解離あり。原則として「緊急手術」の適応。
- Stanford B型:上行大動脈に解離なし。原則として「内科的待機療法(安静・降圧)」だが、合併症があれば緊急介入。
- 診断の要:突発する激しい胸背部痛。造影CTが確定診断に必須。Dダイマー 0.5μg/mL未満は除外に有用。
- 内科的管理:急性期・慢性期ともに収縮期血圧 120〜130mmHg未満の厳格な降圧が予後を左右する。
- 慢性期の管理:偽腔径の拡大(最大径 60mm以上など)に注意し、定期的なCTフォローを行う。
概要・疫学
大動脈解離は、大動脈壁の中膜が裂け、内膜と外膜の間に血液が入り込むことで「真腔」と「偽腔」の二腔構造となる致死的疾患である。発症からの時間経過(急性・慢性)と、解離の範囲(Stanford分類)によって治療戦略が大きく異なる。
急性大動脈解離は、発症から24時間以内の死亡率が極めて高く、1時間ごとに致死率が1〜2%上昇する。高齢者、高血圧患者に多く、冬季や早朝の発症が多い傾向にある。近年、慢性期に偽腔が拡大して大動脈瘤化する症例の管理も重要視されている。
症状・身体所見
- 突発的な激痛:「バットで殴られたような」「引き裂かれるような」と表現される激痛が、発症の瞬間に最大となるのが特徴。
- 移動する痛み:解離の進展に伴い、痛みが胸から背中、腹部へと移動することがある。
- 分枝閉塞症状:頸動脈(脳梗塞)、冠動脈(心筋梗塞)、腹部内臓動脈(腹痛)、下肢動脈(冷感・疼痛)の虚血症状。
- 身体所見:四肢の脈拍不整・血圧左右差(20mmHg以上)、新規の心雑音(大動脈弁閉鎖不全症:ARによる)。
初期検査・鑑別診断
初期検査:
- Dダイマー:0.5μg/mL未満であれば、大動脈解離をほぼ否定できる(感度が極めて高い)。
- 心電図・心エコー:急性冠症候群との鑑別、心嚢水の有無、大動脈弁逆流の評価。
- 造影CT:確定診断のゴールドスタンダード。解離の範囲(Stanford分類)、真腔・偽腔の区別、分枝血流を評価する。
鑑別診断:
専門医へのコンサル基準
- 急性大動脈解離(Stanford A型・B型問わず)を疑った時点で、直ちに心臓血管外科・循環器内科へコンサル。
- Stanford B型で経過観察中、腹痛(腸管虚血)や下肢虚血症状、コントロール不良な疼痛が出現した場合。
- 慢性期フォロー中の解離性大動脈瘤において、瘤径が55〜60mmを超えた場合、または半年で5mm以上の拡大を認める場合。
大動脈解離の診療フローチャート
急性大動脈解離
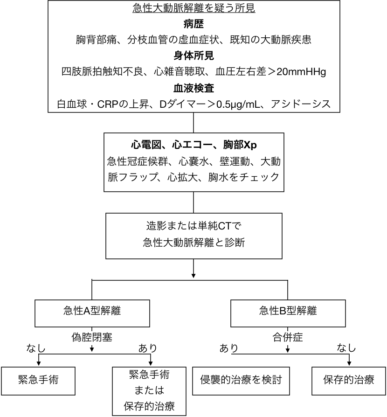
慢性大動脈解離

診断基準・精査の詳細
Stanford分類と治療選択
- Stanford A型(上行解離あり):心タンポナーデ、急性心不全、冠動脈閉塞のリスクが高いため、原則「緊急手術(上行大動脈置換術など)」を行う。
- Stanford B型(上行解離なし):「非複雑型」であればICUでの安静・降圧療法が原則。「複雑型(分枝虚血、破裂、難治性疼痛あり)」ではステントグラフト(TEVAR)や手術を検討する。
慢性期のCTフォロー
初診3〜6ヶ月後に再検し、その後は径の変化に応じて1年〜半年ごとに行う。瘤径 60mm以上は外科的治療の適応基準となる。
治療法・具体的な処方例
急性期の治療
1. 迅速な血圧・心拍数管理
急性期の血圧管理は、解離の進展や破裂を防ぐために最も重要である。収縮期血圧100〜120mmHg、心拍数60bpm以下を目標とし、速やかに静注薬による導入を行う。
- 降圧薬(静注):カルシウム拮抗薬が第一選択となる。
例)ニカルジピン(ペルジピン®)持続静注:0.5〜10μg/kg/minで調節。 - 心拍数管理(β遮断薬):dP/dt(左室収縮速度)を抑制し、大動脈壁への衝撃を和らげる。
例)ランジオロール(オノアクト®)1〜10μg/kg/minで持続静注。
例)エズモロール(ブレビブロック®)25〜200μg/kg/minで持続静注。
2. 厳格な鎮痛・鎮静
疼痛は交感神経を刺激し、血圧・心拍数を上昇させる。発症直後から強力な除痛を行う。
- 鎮痛薬:麻薬性鎮痛薬を躊躇せず使用する。
例)モルヒネ 2〜5mg または フェンタニル 25〜50μg を適宜静注。 - 鎮静薬:疼痛管理が困難な場合や、不穏状態では鎮静薬を併用する。
例)デクスメデトミジン(プレセデックス®)やプロポフォールによる持続鎮静。
3. 外科的介入・血管内治療の判断
分類および合併症の有無(Complicatedか否か)により、治療方針を決定する。
- Stanford A型:診断即、人工血管置換術(上行大動脈置換、あるいは弓部置換)を原則とする。心タンポナーデ合併時は心嚢穿刺を考慮するが、再貯留しやすいため根治術を急ぐ。
- Stanford B型(Complicated):破裂、切迫破裂、臓器虚血(Malperfusion)、難治性疼痛、コントロール不良な高血圧を伴う場合は、緊急〜準緊急でステントグラフト内挿術(TEVAR)や窓形成術(Fenestration)、バイパス術を検討する。
- Stanford B型(Uncomplicated):強力な降圧・安静療法(Medical therapy)を継続する。ただし、偽腔径が大きく(>35-40mm)エントリーが上行に近い症例などは、将来の瘤化リスクが高いため、準急性期のTEVAR介入を検討するケースが増えている。
4. 臓器虚血(Malperfusion)への対応
分枝血管が解離に巻き込まれ、脳、内臓、下肢に血流障害が出現した場合、単なる降圧だけでは不十分である。灌流圧を維持しつつ、ステント留置による再疎通やバイパス術による血流確保を最優先で行う。
慢性期の血圧管理
再解離や瘤化を防ぐため、130/80mmHg未満(可能であれば120mmHg未満)を目指す。β遮断薬はイベント抑制効果が報告されており、優先的に使用される。
【処方例】
- β遮断薬:
ビソプロロールフマル酸塩(メインテート®)2.5mg〜5mg 1錠 分1 朝食後 - ARB:(β遮断薬で不十分な場合)
テルミサルタン(ミカルディス®)40mg 1錠 分1 朝食後 - 脂質異常症(スタチン):
ロスバスタチン(クレストール®)2.5mg 1錠 分1 夕食後
resi Dr.の眼(Pitfalls・匙加減)
「Dダイマー陰性の罠」:Dダイマーは極めて感度が高いが、偽腔閉塞型(ULP型など)の初期には上昇が軽微なことがある。臨床的に強く疑うなら、Dダイマーが低値でも造影CTを躊躇してはならない。
「B型は安心ではない」:Stanford B型は内科治療が原則だが、急性期の死亡率は10%程度あり、決して「軽症」ではない。特に「偽腔が開存している(Patent False Lumen)」症例や、初期の瘤径が大きい症例は、慢性期に高確率で瘤化するため、より厳格な降圧(120mmHg未満)が求められる。
予後・患者説明のポイント
「この病気は血管の壁が剥がれてしまった状態で、再発や破裂のリスクと生涯付き合っていく必要があります」と伝え、継続的な通院と血圧管理の重要性を説く。「痛みがない=治った」ではないことを強調し、特に重いものを持つのを控える、排便時にいきまない、などの生活指導も併せて行う。慢性期には「解離性大動脈瘤」への移行を監視するため、CT検査を欠かさないよう説明する。
参考文献
- 日本循環器学会:2020年改訂版 大動脈瘤・大動脈解離診療ガイドライン

